विषय
मुख्य अंतर
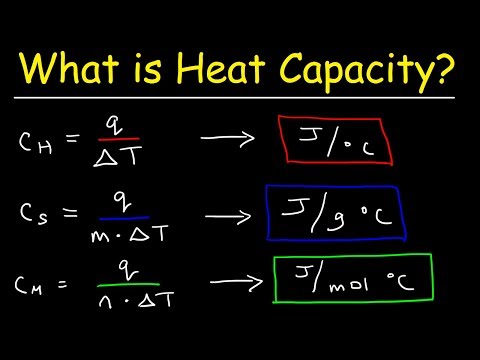
गर्मी ऊर्जा के रूप में से एक है, जब दो वस्तुएं इस ऊर्जा को एक शरीर से दूसरे शरीर में पारित करने की बातचीत करती हैं, तो इसकी संभावना बहुत अधिक होती है। ताप ऊर्जा सीधे तापमान के आनुपातिक होती है, इसका मतलब है कि तापमान में वृद्धि स्वचालित रूप से शरीर के भीतर गर्मी ऊर्जा में वृद्धि को खींच लेगी और इसके विपरीत। इन दोनों शब्दों, विशिष्ट ऊष्मा और ऊष्मा क्षमता का उपयोग ऊष्मागतिकी में व्यापक रूप से किया जाता है क्योंकि दोनों किसी वस्तु के तापमान में वृद्धि करने के लिए आवश्यक ऊर्जा को संदर्भित करते हैं। विशिष्ट ऊष्मा और ऊष्मा की क्षमता विशिष्ट ऊष्मा में अतिरिक्त परिवर्तन के अंतर के साथ एक दूसरे के समान होती है। हालाँकि बहुत से लोग इन शब्दों का परस्पर उपयोग करते हैं क्योंकि उनकी अवधारणा को सामूहिक रूप से 'विशिष्ट ताप क्षमता' के रूप में वर्णित किया गया है। इन दोनों शब्दों के बीच अंतर प्राप्त करने के लिए किसी को विशिष्ट गर्मी में अतिरिक्त चर के बारे में जानने की आवश्यकता है। ऊष्मा क्षमता किसी पदार्थ के तापमान को 1 डिग्री सेल्सियस (°) तक बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा हैसी) या 1 केल्विन, जबकि विशिष्ट ऊष्मा की मात्रा है, जो पदार्थ के तापमान को बढ़ाने के लिए 1 किग्रा।सी) या 1 केल्विन।
तुलना चार्ट
| विशिष्ट ताप | ताप क्षमता | |
| परिभाषा | विशिष्ट गर्मी 1 डिग्री सेल्सियस (डिग्री सेल्सियस) या 1 केल्विन द्वारा द्रव्यमान 1kg या 1g वाले पदार्थ के तापमान को बढ़ाने के लिए आवश्यक गर्मी की मात्रा है। | हीट कैपेसिटी किसी पदार्थ के तापमान को 1 डिग्री सेल्सियस (° C) या 1 केल्विन बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा है। |
| द्रव्यमान | विशिष्ट ताप वस्तु या पदार्थ के द्रव्यमान के सीधे आनुपातिक होता है। | ताप क्षमता द्रव्यमान पर निर्भर नहीं करती है। |
| एस आई यूनिट | जे किलो-1 क-1 | जम्मू / कश्मीर |
विशिष्ट गर्मी क्या है?
विशिष्ट ऊष्मा ऊष्मा क्षमता से बहुत मिलती-जुलती है, क्योंकि दोनों में एक शरीर में तापमान में वृद्धि की एक इकाई को शामिल करना शामिल है, हालांकि यह उत्तरार्द्ध के साथ भिन्न होता है क्योंकि इसमें एक अतिरिक्त चर होता है, 'मास' को ध्यान में रखते हुए देखा जाता है। तापमान में वृद्धि की एक इकाई। पानी की विशिष्ट गर्मी 4.186 Jg है-1oसी-1, आसान शब्दों में हम कह सकते हैं कि 1 की वृद्धि करने के लिए ओ1 ग्राम पानी में C के लिए हमें 4.186 जूल ताप ऊर्जा की आवश्यकता होती है। गर्मी और तापमान के बीच के संबंध को इस प्रकार व्यक्त किया जा सकता है:
क्यू = सेमी =T,
कहाँ पे,
क्यू गर्मी है जोड़ा गया
सी विशिष्ट गर्मी है
∆T तापमान में परिवर्तन है
जब चरण परिवर्तन का सामना करना पड़ता है, तो संबंध वैध नहीं रहता है, मतलब पानी को गैसीय अवस्था (क्वथनांक) में बदलना या जब बर्फ तरल अवस्था (गलनांक) में परिवर्तित हो जाता है। यह इसलिए है क्योंकि चरण परिवर्तन के दौरान गर्मी को हटा दिया जाता है या जोड़ा जाता है। तापमान में बदलाव नहीं लाना। जब यह सैद्धांतिक या प्रयोगशाला के काम के बारे में होता है, तो गर्मी की क्षमता के बजाय विशिष्ट गर्मी का उपयोग किया जाता है क्योंकि यह पदार्थ या वस्तु के द्रव्यमान को भी मापता है।
हीट कैपेसिटी क्या है?
हीट कैपेसिटी किसी पदार्थ के तापमान को 1 डिग्री सेल्सियस (° C) या 1 केल्विन बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा है। तापमान में वृद्धि या तापमान में वृद्धि से पदार्थ के द्रव्यमान के साथ कुछ भी नहीं होता है। ताप ऊर्जा सीधे तापमान के आनुपातिक होती है, इसका मतलब है कि तापमान में वृद्धि स्वचालित रूप से शरीर के भीतर गर्मी ऊर्जा में वृद्धि को खींच लेगी और इसके विपरीत। हीट कैपेसिटी को इस समीकरण के उपयोग से परिभाषित किया जा सकता है:
C = /Q / ∆T,
कहाँ पे,
Δ Q ऊष्मा की मात्रा है
C विशिष्ट HEAT है
Change T तापमान में परिवर्तन है
विशिष्ट गर्मी बनाम हीट क्षमता
- हीट कैपेसिटी किसी पदार्थ के तापमान को 1 डिग्री सेल्सियस (° C) या 1 केल्विन तक बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा है, जबकि विशिष्ट ऊष्मा उस द्रव्यमान की मात्रा को बढ़ाने के लिए आवश्यक है जिसके द्रव्यमान का द्रव्यमान 1kg या 1g 1 डिग्री हो। सेल्सियस (° C) या 1 केल्विन।
- विशिष्ट ताप वस्तु या पदार्थ के द्रव्यमान के सीधे आनुपातिक होता है, जबकि गर्मी की क्षमता द्रव्यमान पर निर्भर नहीं करती है।
- J / K ऊष्मा क्षमता की SI इकाई है, जबकि J kg-1 क-1 विशिष्ट ऊष्मा के लिए SI इकाई है।


